Você se pergunta quantos elementos tem a tabela periódica em 2026? É comum a gente se deparar com essa dúvida, afinal, é um conhecimento fundamental para entender a química. Mas a resposta é mais direta do que parece, e eu vou te contar tudo. Vamos desmistificar esse universo e mostrar como a tabela periódica atual é completa e fascinante.
A contagem exata de quantos elementos tem a tabela periódica e o que isso significa para nós em 2026
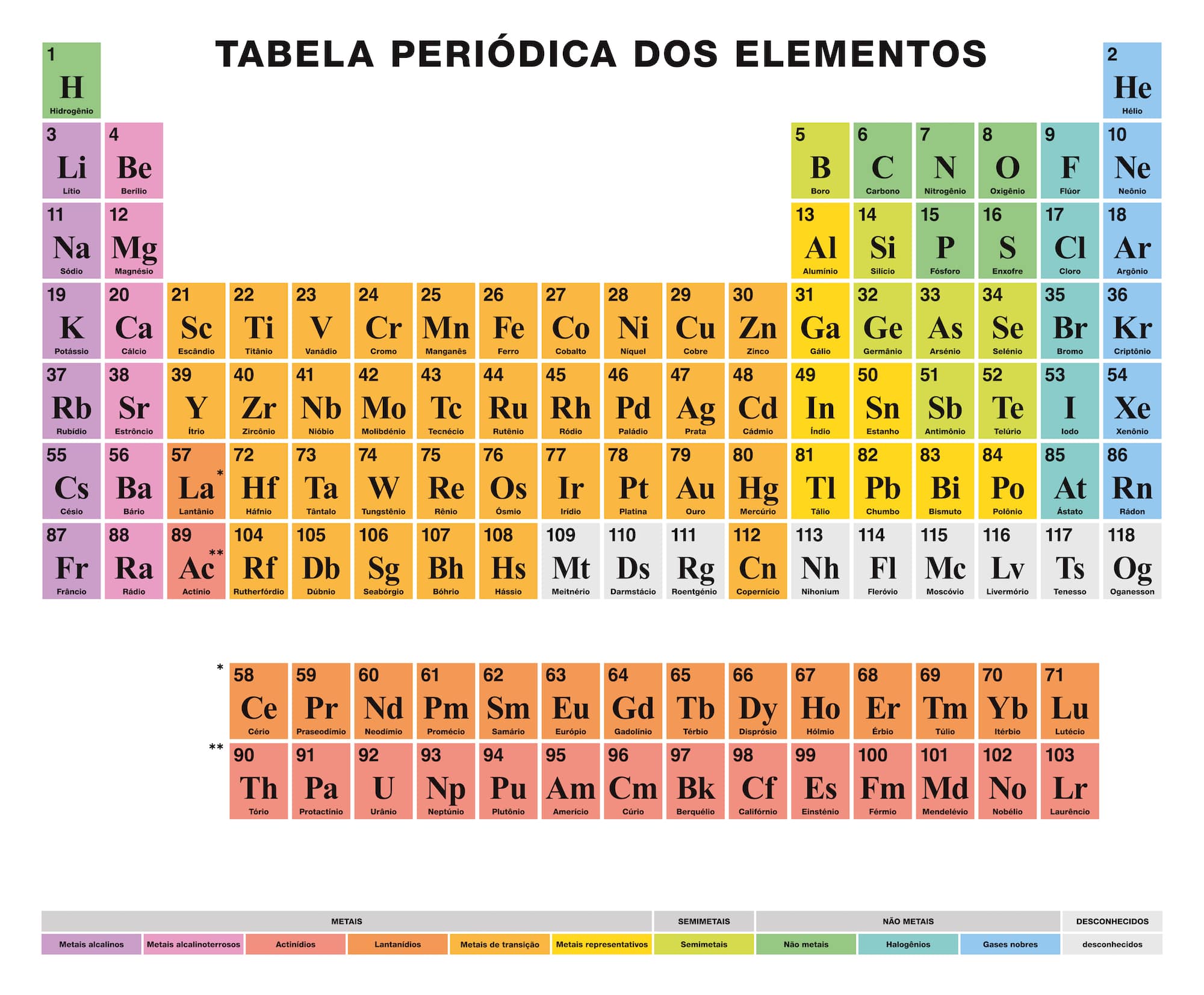
Atualmente, a tabela periódica que usamos em 2026 conta com 118 elementos. Sim, são exatamente esses 118 que compõem a base de tudo o que conhecemos na química. Esse número representa um marco, com todos os elementos dos sete primeiros períodos já confirmados e organizados.
O último a ter seu lugar garantido foi o Oganessônio (Og), com o número atômico 118. É ele que fecha a sétima linha da tabela.
A organização dessa lista não é por acaso. Ela segue uma lógica clara baseada no número atômico e nas propriedades de cada elemento. Isso facilita demais na hora de prever como eles vão se comportar.
“A tabela periódica atual possui 118 elementos confirmados, sendo o Oganessônio (Og) o último elemento com número atômico 118.”
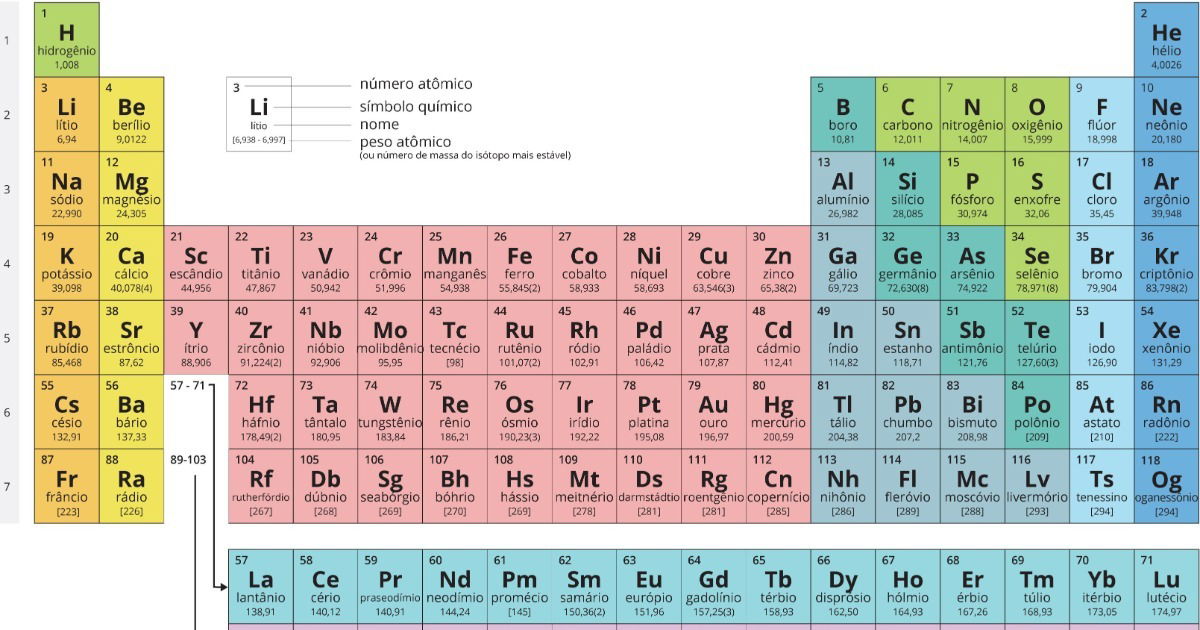
O que é e para que serve a Tabela Periódica em 2026?
A tabela periódica é uma ferramenta fundamental para qualquer pessoa que se interesse por ciência, especialmente a química. Ela organiza os elementos químicos conhecidos de uma forma lógica e visualmente clara, baseada em suas propriedades e número atômico. Pense nela como um mapa que nos ajuda a entender o comportamento da matéria.
Em 2026, continuamos a usar essa organização para prever como novos elementos podem se comportar e para entender as reações químicas que ocorrem ao nosso redor, desde o preparo de uma refeição até o funcionamento de tecnologias avançadas. É um guia essencial que facilita o estudo e a pesquisa científica.
| Característica | Detalhe |
| Total de Elementos Confirmados | 118 |
| Último Elemento Confirmado | Oganessônio (Og) |
| Número Atômico do Último Elemento | 118 |
| Períodos Completos na Tabela | 7 |
| Princípio de Organização | Propriedades e Número Atômico |
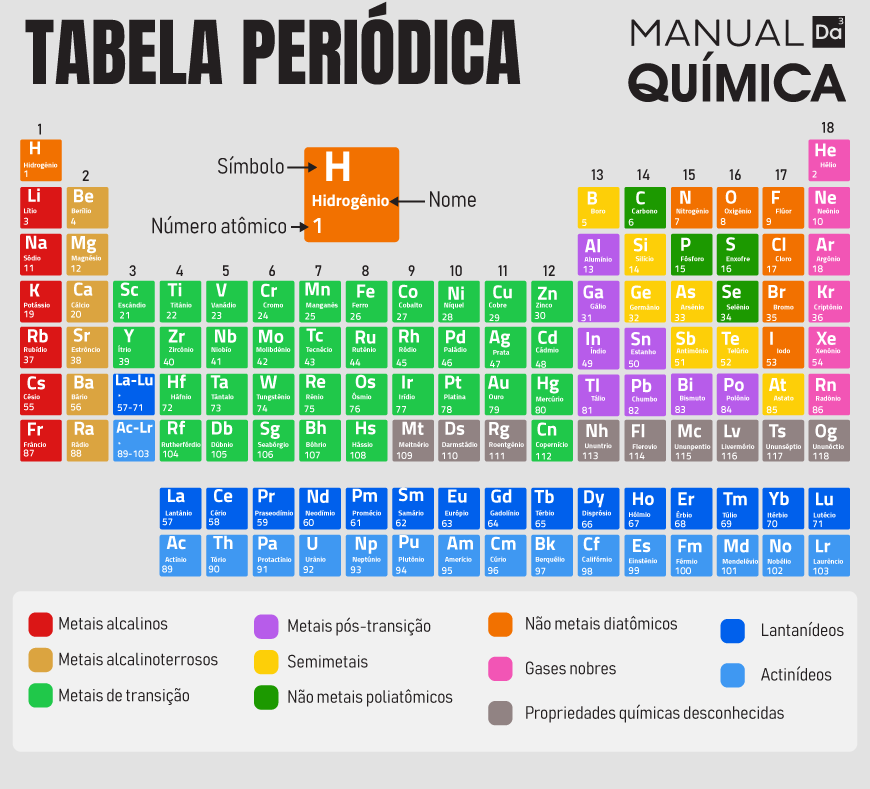
O Número Total de Elementos na Tabela Periódica
Atualmente, em 2026, a tabela periódica reconhece oficialmente 118 elementos. Essa contagem representa todos os elementos que foram descobertos ou sintetizados e cujas propriedades foram confirmadas pela comunidade científica internacional. Cada um desses elementos possui características únicas que os distinguem, mas que também compartilham padrões quando organizados corretamente.
A jornada para chegar a esses 118 elementos foi longa, abrangendo séculos de descobertas e avanços tecnológicos. A busca por novos elementos continua, impulsionada pela curiosidade humana e pela busca por materiais com propriedades inéditas.
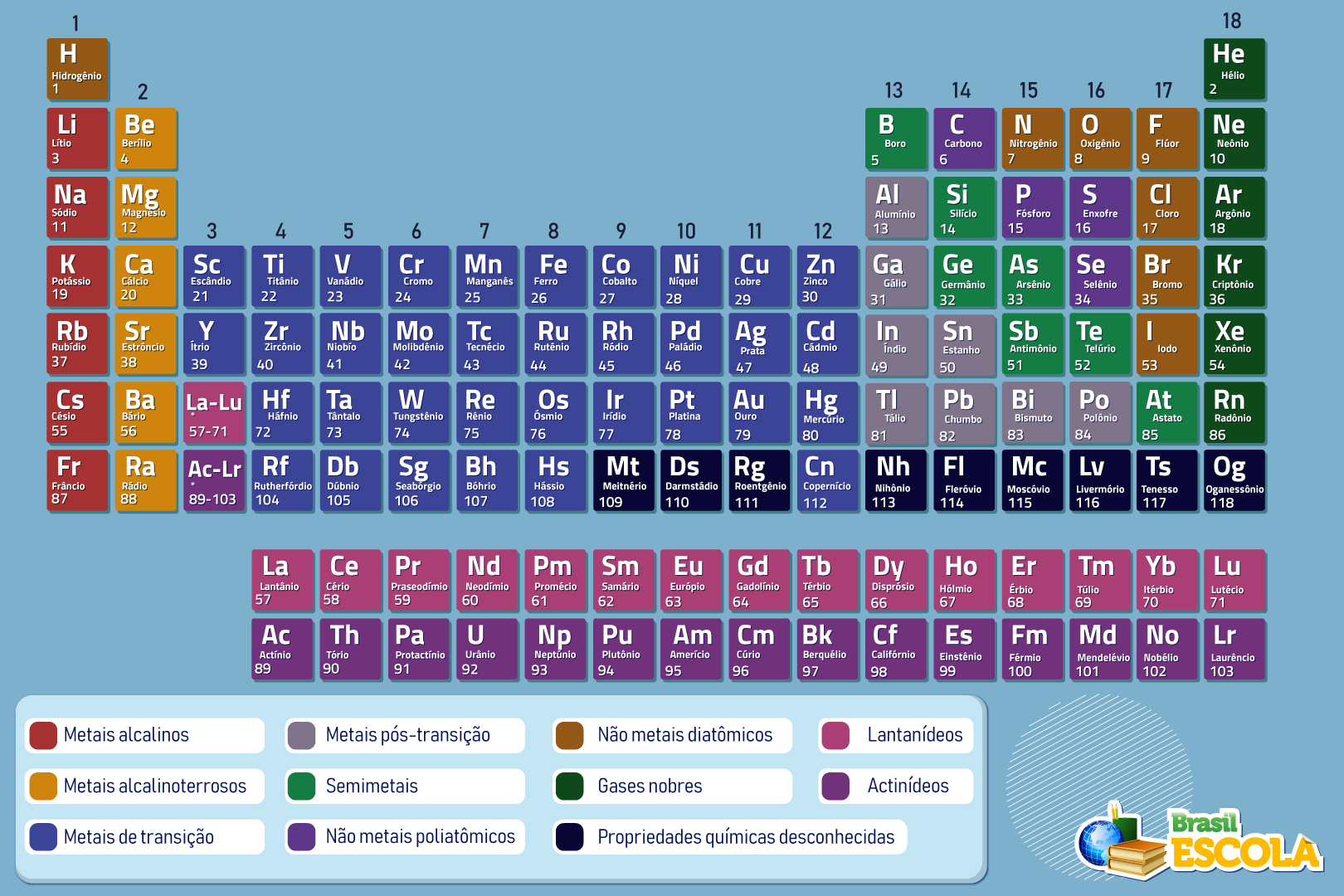
Oganessônio (Og): O Último Elemento Confirmado
O Oganessônio (Og), com o número atômico 118, detém o posto de último elemento oficialmente adicionado à tabela periódica. Sua síntese foi um marco significativo, completando a sétima linha da tabela. Elementos com números atômicos tão altos são geralmente instáveis e de curta duração, sendo produzidos em laboratório sob condições muito específicas.
A confirmação do Oganessônio foi um processo rigoroso, envolvendo a reprodução de experimentos e a verificação de suas propriedades decaimento. Ele pertence ao grupo dos gases nobres, embora suas propriedades possam divergir dos membros mais leves do grupo devido a efeitos relativísticos.
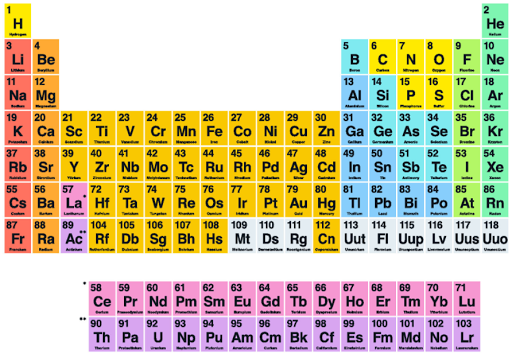
A Organização da Tabela Periódica em Períodos
A organização da tabela periódica em períodos, que são as linhas horizontais, é crucial. Cada período representa um nível de energia principal onde os elétrons de um átomo estão localizados. À medida que avançamos de um período para o outro, um novo nível de energia eletrônica é preenchido.
O número de elementos em cada período aumenta à medida que descemos na tabela. Isso ocorre porque os períodos mais baixos acomodam subníveis de energia mais complexos, permitindo a inclusão de mais elementos com propriedades distintas. Essa estrutura sequencial é uma das chaves para entender as tendências periódicas.

Grupos Específicos da Tabela Periódica e Suas Características
As colunas verticais da tabela periódica são chamadas de grupos. Elementos dentro do mesmo grupo geralmente compartilham um número semelhante de elétrons em sua camada mais externa, o que lhes confere propriedades químicas muito parecidas. Vamos explorar alguns grupos notáveis:
Os metais alcalinos (Grupo 1, exceto o hidrogênio) são altamente reativos, macios e têm baixa densidade. Já os metais alcalino-terrosos (Grupo 2) são também reativos, mas um pouco menos que os do Grupo 1. Os halogênios (Grupo 17) são não-metais muito reativos que formam sais quando reagem com metais. Por fim, os gases nobres (Grupo 18) são conhecidos por sua inércia química, pois possuem sua camada de valência completa.
A semelhança nas propriedades dos elementos de um mesmo grupo é um dos pilares da previsibilidade da tabela periódica.
Como os Elementos são Descobertos e Sintetizados
A descoberta de elementos pode ocorrer de duas formas principais: pela descoberta em fontes naturais ou pela síntese em laboratório. Elementos mais leves, como o hidrogênio e o hélio, foram formados nos primórdios do universo. Elementos mais pesados, até o urânio, são encontrados na natureza, embora muitos precisem ser extraídos e purificados.
Para elementos com número atômico muito alto, a síntese laboratorial é o caminho. Isso envolve a colisão de núcleos atômicos em aceleradores de partículas. O processo é complexo e os elementos resultantes geralmente têm uma meia-vida extremamente curta, exigindo técnicas avançadas para sua detecção e confirmação. A pesquisa em pesquisa e desenvolvimento nuclear é fundamental nesse aspecto.
A Importância do Número Atômico na Classificação
O número atômico é a pedra angular da organização da tabela periódica. Ele representa a quantidade de prótons no núcleo de um átomo e, em um átomo neutro, é igual ao número de elétrons. Essa simples contagem determina a identidade de um elemento.
Ao organizar os elementos em ordem crescente de número atômico, observamos um padrão recorrente em suas propriedades químicas e físicas. Essa periodicidade é o que confere à tabela seu poder preditivo e explicativo, permitindo que cientistas antecipem o comportamento de elementos ainda não totalmente estudados.
Os 7 Períodos da Tabela Periódica e Seus Elementos
A tabela periódica atual em 2026 é composta por sete períodos completos, cada um correspondendo a um nível de energia principal. O primeiro período é o mais simples, contendo apenas dois elementos: hidrogênio (H) e hélio (He). Já o sexto e o sétimo períodos são os mais extensos, incluindo os lantanídeos e os actinídeos, respectivamente.
Cada período introduz novos subníveis eletrônicos que são preenchidos, resultando em uma diversidade crescente de propriedades. Entender a estrutura de cada período é essencial para compreender as transições de propriedades observadas ao longo da tabela.
Propriedades e Tendências dos Elementos Químicos
A beleza da tabela periódica reside nas tendências periódicas que ela revela. Propriedades como raio atômico, energia de ionização, eletronegatividade e afinidade eletrônica variam de maneira previsível ao longo dos períodos e grupos. Por exemplo, o raio atômico geralmente diminui ao longo de um período e aumenta ao longo de um grupo.
Essas tendências não são meras curiosidades; elas explicam por que certos elementos reagem de forma mais vigorosa que outros, ou por que formam determinados tipos de compostos. O estudo dessas tendências é vital para a química, permitindo o design racional de novos materiais e processos. Para mais detalhes sobre a descoberta de elementos, a IUPAC é uma referência importante: IUPAC Periodic Table.
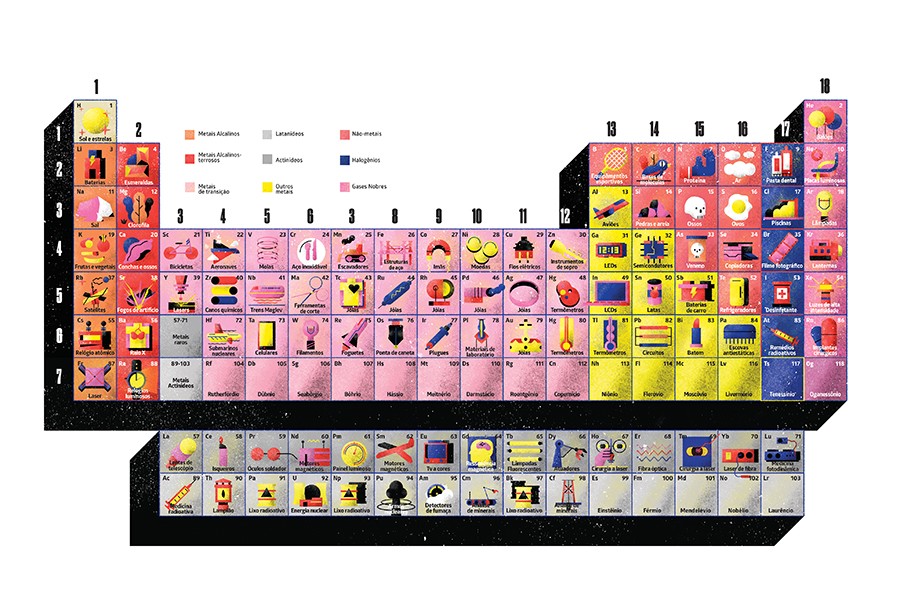
Conclusão: A Tabela Periódica em 2026
Em suma, a tabela periódica em 2026 continua sendo uma obra-prima da organização científica, com seus 118 elementos perfeitamente arranjados. Ela não é apenas um registro de descobertas, mas uma ferramenta dinâmica que guia a pesquisa e a inovação. A compreensão de sua estrutura e das propriedades dos elementos que ela contém é indispensável para quem deseja desvendar os segredos do universo material.
O estudo contínuo e a busca por novos elementos garantem que a tabela periódica permaneça um campo fértil para descobertas futuras, reafirmando seu papel central na ciência. A exploração de elementos superpesados, como os que se estendem além do Oganessônio, é uma fronteira ativa na física e química nuclear, com potencial para revelar novas leis da natureza. A Agência Brasileira de Desenvolvimento Industrial (ABDI) também aborda a importância da ciência e tecnologia: Inovação e Desenvolvimento Tecnológico no Brasil.
Dicas Extras
- Fique de olho nas descobertas: A ciência não para! Novos elementos podem ser sintetizados e confirmados. Acompanhar as notícias científicas é um ótimo jeito de saber se a tabela vai aumentar.
- Entenda a organização: Saber como a tabela periódica é organizada, com seus grupos e períodos, ajuda a prever as propriedades dos elementos, mesmo os recém-descobertos.
- Estude as características: Cada elemento tem suas particularidades. Mergulhar nas características dos elementos químicos da tabela periódica e suas propriedades torna o estudo mais interessante e prático.
Dúvidas Frequentes
Quantos elementos tem a tabela periódica atualmente?
Atualmente, a tabela periódica contém 118 elementos confirmados e reconhecidos oficialmente. Todos eles preenchem as sete primeiras linhas da tabela.
Qual o último elemento adicionado à tabela periódica?
O último elemento confirmado é o Oganessônio (Og), com número atômico 118. Ele fecha a sétima linha da tabela periódica.
Como os novos elementos são descobertos ou criados?
Novos elementos, especialmente os mais pesados, geralmente são sintetizados em laboratórios através de colisões de átomos em aceleradores de partículas. A confirmação e nomeação são processos rigorosos feitos por órgãos internacionais.
Conclusão
É fascinante acompanhar a evolução da ciência e como a tabela periódica se completa. Com 118 elementos confirmados, ela é uma ferramenta poderosa para entender o universo. Continuar explorando a organização dos elementos na tabela periódica e se aprofundar em como a tabela periódica é organizada pode abrir novas perspectivas. Quem sabe o que mais a química nos reserva?

